Tværgående fagforum: Behandling med antistoffer
Pharma 04/2023
Esther Breij, Genmab, var oplægsholder på Pharmadanmarks seneste arrangement i det tværgående fagforum ’Nye lægemiddelmodaliteter i dag og i fremtiden’. Hun tog deltagerne med på rejsen fra opdagelsen af antistoffer over virkningsmekanismer til et indblik i udviklingen af antistoffer til behandling af cancer hos Genmab.
Af Hanne Arentsen, chefkonsulent, Pharmadanmark
Pharmadanmarks fagforum om nye lægemiddelmodaliteter – i dag og i fremtiden har siden opstarten sidste år beskrevet nogle af de videnskabelige landvindinger i forskningen og udviklingen af nye behandlinger, blandt andet cellebaserede terapier.
På det seneste fagforum 17. april var emnet antistoffer og antistofbehandling, og Esther Breij, Vice President, Global Head of Translational Research hos Genmab, gav deltagerne et spændende indblik i historien bag brugen af antistoffer, den nuværende brug og i potentialet på længere sigt.
Siden Von Behring i 1890'erne opdagede princippet bag antistoffer ved at immunisere mus med difteri-toxin, er antistofbehandling blevet en af de vigtigste behandlingsformer i lægemiddelvidenskaben.
I starten benyttede man sig primært af dyr såsom mus, hvor man inficerede dyrene, og benyttede det immuniserede antiserum til behandling. Den animalske oprindelse medførte dog lav human kompatibilitet og immunisering hos mennesker.
I dag fokuserer forskning i antistoffer særligt på enten at indsætte humane sekvenser i antistoffer fra dyr (humanisering) eller via antistoffer udtrykt i mammale celler. Det har medført, at den humane kompatibilitet er større og risikoen for uønsket immunrespons er lavere.
Antistofbehandling vinder terræn
Flere og flere af de lægemidler, der udvikles på verdensplan, er biologiske lægemidler, og inden for disse er det i særdeleshed antistof-baseret behandling, der vinder terræn.
På listen over de ti mest solgte lægemidler globalt i 2023 (Figur 1) finder man fem antistoffer: Keytruda (pembrolizumab), Humira (adalimumab), Opdivo (nivolumab), Dupixent (dupilumab) og Stelara (ustekinumab), som alle behandler cancer eller immunsygdomme, og som alle er baseret på IgG antistoffer.
Antistoffer udmærker sig ved deres høje specificitet. Dette gør dem velegnede til for eksempel cancerbehandling, hvor der er behov for at målrette behandlingen mod cancerceller.
En anden fordel ved antistoffer er, at de ofte har en lang halveringstid, for eksempel 21 dage. Det medfører, at patienterne ikke skal behandles ofte. Dette er en fordel, idet antistoffer ikke kan administreres oralt, men skal indgives ved intravenøs eller subkutan administration.
Fremstilling og oprensning af antistoffer er i dag en veldefineret proces. Den oftest benyttede cellelinje er CHO (Chinese Hamster Ovary), som er i stand til at producere antistoffer med komplekse modifikationer og glykosyleringer, som ligner de humane. 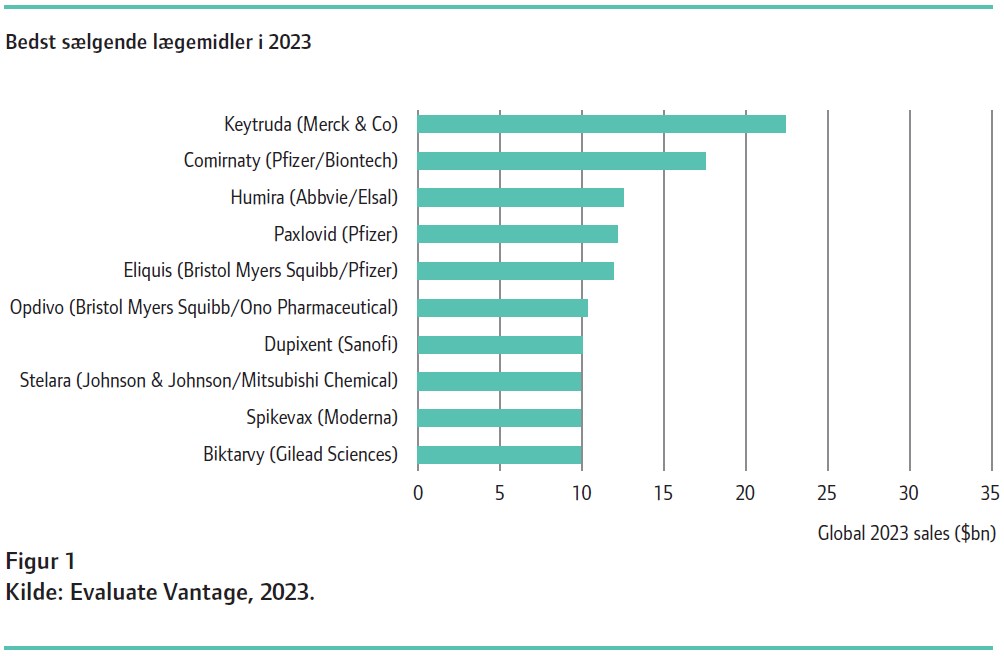
Immunterapi
Immunterapi er en terapiform, hvor kroppens eget immunsystem stimuleres til at angribe eller blokere cancerceller. Målet med immunterapi er oftest ikke at helbrede, men at forbedre livskvaliteten for cancerpatienter, så de kan leve med deres sygdom, uden at den definerer hele deres liv.
En af de nyere og banebrydende behandlingsregimer inden for immunterapi er checkpoint inhibition. Checkpoints er membranproteiner, der udtrykkes på overfladen af blandt andet T-celler, og som nedregulerer immunforsvaret ved stimulering.
Formålet er at undgå, at immunresponset bliver så kraftigt, at det dræber raske celler i kroppen. Cancerceller kan beskytte sig selv mod angreb ved, at ligander på deres celleoverflade binder sig til checkpoints og derved hæmmer immunforsvaret. Checkpoint inhibitors blokerer for, at cancercellernes ligander kan binde til checkpoints og bevirker derved, at immunforsvaret genaktiveres og dræber cancercellen.
Det første checkpoint inhibition lægemiddel til behandling af cancer, Yervoy (ipilimumab), blev godkendt i 2011, og en række andre produkter er sidenhen godkendt. Der forskes fortsat intensivt i checkpoint inhibitors. 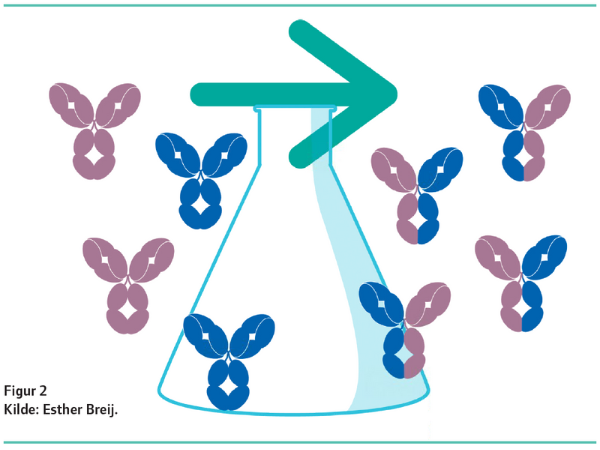
| Hvad er antistoffer? Antistoffer er en essentiel komponent i immunsystemet og spiller en vital rolle i kroppens forsvar mod infektionssygdomme. Antistoffer produceres i B-lymfocytter, og er specifikt designet til at genkende og neutralisere fremmede stoffer såsom bakterier, vira og andre toksiner. Antistoffer er store Y-formede proteinkomplekser, der består af fire proteinkæder: To længere heavy chains og to kortere light chains, som er forbundet med disulfidbroer. Den øverste del af antistoffet (Fab-regionen) bestemmer antistoffets specificitet overfor bestemte antigener. Den nederste del af antistoffet (Fc-regionen) er den del af antistoffet, som interagerer med celleoverfladens Fc-receptorer. Det er Fc-regionen, der bestemmer hvilken klasse antistoffet tilhører, og mens Fc-regionen mellem klasserne er forskellige, er den konstant indenfor klassen. Der findes fem større klasser af antistoffer hos mennesker: IgG, IgA, IgM, IgE og IgD. IgA er primært associeret med tarmsystemet, mens IgE, som også er det antistof, der udgør den mindste del af det totale antistofindhold i serum, spiller en stor rolle i kroppens allergiberedskab. Det er antistoffer af klassen IgG, der er dominerende i kroppen, og cirka 80 procent af det totale antistofindhold i serum består af IgG antistoffer. IgG antistoffer er relativt lette at fremstille. De fleste godkendte antistof-baserede lægemidler tilhører IgG klassen. |
Et indblik i Genmabs forskning i antistoffer
Esther Breij sluttede oplægget af med at give et lille indblik i forskningen i antistoffer hos Genmab:
Konjugerede antistoffer – tisotumab vedotin
Et af de områder, som Genmab forsker i, er ADC (antibody-drug conjugates), det vil sige konjugering af aktive substanser på antistoffer til cancerbehandling. Det giver mulighed for at benytte antistoffet som transportør af cellegiften/toksinet ind i cellen, hvor det frigives og nedbryder cancercellen.
Tivdak (tisotumab vedotin) er et konjugeret IgG1 antistof rettet mod TF (tissue factor), som Genmab har udviklet i samarbejde med det amerikanske firma Seagen, der er specialister inden for ADC. Tissue factor spiller en stor rolle i blodkoagulationskaskaden og menes også at påvirke tumorvækst, angiogenese, metatastase og dannelsen af tromboser hos cancerpatienter.
Konjugatet består af et TF specifikt human monoklonant IgG1 antistof linket via VC (valine-citruline) til MMAE (microtubule-disrupting agent monomethyl auristatin E). MMAE toksinet er et potent antineoplastisk stof, der ikke kan administreres alene på grund af sin toksicitet, og det må derfor nå sit target via konjugering. Når tisotumab vedotin internaliseres i tumorcellens lysosomer, vil VC linket protolyseres, og MMAE frigives fra antistoffet. Det betyder, at MMAE kan dræbe cancercellen indefra via apoptose og hæmning af cellevækst.
Tivdak blev betinget godkendt til behandling af voksne patienter med tilbagevendende eller metastatisk livmoderhalskræft i USA i 2021 på baggrund af resultaterne af et klinisk fase 2 studie i 101 patienter.
Genmab og Seagen er i gang med at udføre et fase 3 studie.
Bispecifikke antistoffer – epcoritamab
IgG4 antistoffer dannes i kroppens B-lymfocytter som monoklonale antistoffer. Selvom antistofferne tilhører den samme klasse, vil der være forskelle i deres Fab-region, og dermed i deres specificitet overfor antigener. I kroppen vil der spontant ske en ombytning af den ene del af Fab-regionen via løse bindinger, så antistoffet vil være i stand til at genkende to forskellige antigener, altså udvise bispecificitet. Potentialet inden for bispecificitet er enormt, og det er denne spontane Fab-exchange, der ligger til grund for udviklingen af bispecifikke antistoffer.
I arbejdet med bispecifikke antistof-lægemidler vil man gerne kontrollere Fab-exchange, så de bindinger, der opstår mellem de ombyttede Fab-regioner er stærke, og bispecificiteten bibeholdes. Genmab benytter sig af den såkaldte DuoBody teknologi, hvor man producerer to IgG1 monoklonale antistoffer med forskellig specificitet, men matchende mutationer i Fc-regionen. Når de to antistoffer kombineres, vil de matchende mutationer medføre kontrolleret Fab-exchange, og dermed opnås et nyt antistof med bispecificitet (se figur 2).
Epcoritamab er et humaniseret bispecifikt antistof, som har specificitet for både CD3 overfladeproteiner på T-celler og CD20 overfladeproteiner på maligne B-celler. Epcoritamab forårsager dermed T-celle medieret nedbrydning af CD20 positive B-celler, fordi antistoffet bindes til både CD3 og CD20, grundet sin bispecificitet. Epcoritamab er under klinisk udvikling, og resultaterne af et fase 1/2 studie af 157 patienter blev publiceret i JCO i december 2022.
Resultaterne viste, en responsrate på 63,1 procent i patienter med storcellet B-celle lymfom hvoraf 38,9 procent af patienterne opnåede komplet respons. Behandlingen var veltolereret. Baseret på disse fund er data for epcoritamab indsendt til regulatoriske myndigheder verden over og er aktuelt under vurdering med henblik på godkendelse.
Fremtidige møder i fagfora
Oplægget blev modereret af Kristian Strømgaard, professor ved Faculty of Health and Medical Sciences ved Københavns Universitet og Lead på Center of Biopharmaceuticals. Det er ham, der er garant for det faglige indhold på det tværgående fagforum i nye lægemiddelmodaliteter.
Det næste oplæg kommer til at omhandle genterapi, og afholdes i september.
Pharmadanmark har også et nyt fagforum under opstart. Det omhandler ’digitalisering i life science’, og det første oplæg om kunstig intelligens afholdes 22. maj.
Du kan stadig nå at tilmelde dig til arrangementet via Minside her.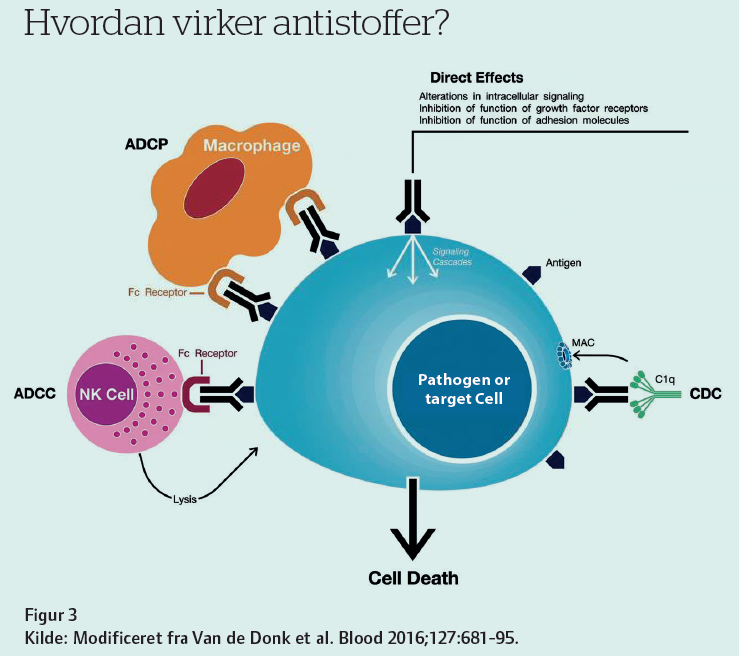
|
ADCC (antistof-afhængig cellulær cytotoksicitet) respons: Når antistoffet binder sig til antigenet på cellen, genkendes det af NK (natural killer) celler, som er cytotoksiske lymfocytter. Binding af NK-celler på antistoffets Fc receptorer aktiverer frigørelse af cytotoksiske granulater, hvilket resulterer i celledød. ADCP (antistof-afhængig cellulær fagocytose) respons: Når antistoffet binder til antigener, dækkes/opsoniseres cellen. Den opsoniserede celle tiltrækker makrofager, der optager og nedbryder cellen via fagocytose. CDC (komplement afhængig cytotoksicitet) respons: Antistof binder på celleoverfladen i strukturer, for eksempel i en hexamerstruktur. Antistofstrukturen genkendes af et C1 proteinkompleks, og ved binding udløses en lang kaskade af proteaser, som munder ud i dannelse af MAC (membrane attack complex). MAC binder sig til cellen og medfører perforering af cellemembranen, og dermed celledød. |







